Диагноз легочной тромбоэмболии (ТЭЛА) не прост даже у небеременных пациенток, и нет исследований, определивших бы оптимальные диагностические подходы в специфической группе беременных. Клиническая диагностика ТЭЛА рассматривает широкий спектр признаков и симптомов, который нередко еще более усложняется физиологическими изменениями при беременности. Диспноэ, тахипноэ и плевральная боль высокочувствительны, но малоспецифичны для ТЭЛА [20]. Другие типичные признаки включают хрипы и крепитацию, тахикардию (> 100 уд./мин), шум трения плевры, и усиление второго тона на легочной артерии при аускультации шумов сердца. В одном из исследований диспноэ и тахипноэ были зафиксированы у 90% пациенток из 383 с ТЭЛА. Диспноэ, тахипноэ или плевральная боль были у 97% [20].
Признаки и симптомы, ассоциирующиеся с ТЭЛА, возможны при широком спектре других острых заболеваний легких. Астма, по-видимому, — наиболее частое заболевание, встречающееся у беременных, далее идут пневмония и отек легких. Пневмония и астма могут развиться на любом сроке беременности или послеродового периода. Отек легких чаще всего наблюдается в конце доношенной беременности и связан с гес- тозом или является результатом избыточного введения жидкости во время родов. Эти состояния обычно исключают на основании анамнеза пациентки и результата рентгенографии грудной клетки.
Такие диагностические исследования, как электрокардиограмма, рентгенография грудной клетки и показатели газов артериальной крови, могут подтвердить диагноз ТЭЛА или идентифицировать другую этиологию жалоб пациентки. Для исключения пневмонии или отека легких следует выполнить рентгенографию грудной клетки в передне-задней и боковой проекциях (с защитой живота). Рентгенография грудной клетки также необходима для точной интерпретации вентиляционно-перфузионного (V/Q) сканирования. Неспецифические изменения, такие как ателектазы, односторонний выпот в плевральной полости, зоны пониженной прозрачности или повышения купола диафрагмы, характерны для пациентов с ТЭЛА, равно как и неспецифические электрокардиографические изменения. Характерный SjQ3T3 паттерн бывает редко.
Большинство клинически значимых эмбол сопровождается гипоксемией (артериальное Рао2 < 85 мм рт. ст.) и расширением или повышением альвеолярно-артериальной разницы по кислороду (Рао2-Рао2 > 20 мм рт. ст.). Тем не менее можно ожидать, что 10-15% пациентов с ТЭЛА будут иметь нормальное Рао2. Во время третьего триместра Рао2 в положении лежа на спине существенно ниже, чем в положении стоя, и разница может достигать 15 мм рт. ст. Таким образом в третьем триместре образцы для исследования газов артериальной крови следует набирать в положении сидя. Опубликованы данные о том, что альвеолярно-артериальная разница по кислороду была < 15 мм рт. ст. у 58% в небольших группах беременных с документированной ТЭЛА, что указывает на ненадежность расчетных скрининговых тестов для диагностики ТЭЛА у беременных.
В настоящее время скрининговым тестом выбора для диагностики легочной эмболии у беременных являются радиоизотопное исследование легких или вентиляционно-перфузионное (V/Q) сканирование. При нормальном результате диагноз ТЭЛА можно исключить. Положительный результат сканирования высокой вероятности является основанием для назначения антикоагулянтов. К сожалению, у большинства пациенток с ТЭЛА результат V/Q сканирования интерпретируется как имеющий низкую или среднюю (неопределимую) вероятность, что потребует выполнения легочной ангиографии или КТ -сканирования легких. Спиральная КТ более чувствительна и дает более однозначно трактуемые результаты, чем V/Q сканирование для диагностики легочной эмболии, но может не выявить субсегментарные эмболы. Диагностическая ценность магнитно-резонансной ангиографии в настоящее время исследуется, но метод исследования также может оказаться недостаточно чувствительным для выявления малых субсегментарных эмболов.
Врачу необходимо следить за тем, чтобы беременная пациентка в процессе рентгенографии грудной клетки, V/Q сканирования и ангиогорафии легких суммарно получила менее 0,5 рад (0,005 кгрей) лучевой нагрузки на плод.
Расчетная лучевая доза только для V/Q сканирования составляет около 0,1 рад. Диагностический алгоритм для выявления ТЭЛА у беременных представлен на рис. 12-2.
Лечение
В настоящее время для лечения ТГВ или ТЭЛА беременных женщин рекомендуется госпитализировать. Всем женщинам со сроком беременности более 12 недель в комплексе первичного обследования необходимо исследовать сердцебиение плода. При жизнеспособном плоде (срок беременности более 24 недель) пациентку следует наблюдать совместно с акушерской бригадой, желательно в условиях постоянного мониторирования плода. Наилучшее лечение для плода — это быстрое восстановление и стабилизация состояния матери. Для предупреждения гипоксемии матери и плода сатурацию крови матери кислородом следует поддерживать на уровне > 95%. Пациенткам с гемодинамическими расстройствами необходим мониторинг в условиях ОРИТ. Если после адекватного возмещения дефицита объема циркулирующей крови гипотензия сохраняется, препаратом выбора для поддержания АД матери > 80 мм рт. ст. считается допамин, хотя прессоры могут еще более ухудшить маточный кровоток У пациенток с высоким риском ТЭЛА лечение антикоагулянтами следует начать еще до подтверждающих диагностических исследований. При необходимости можно использовать такие анальгетики, как морфин.
После подтверждения диагноза венозной тромбоэмболии необходимо быстрое и достаточно длительное лечение антикоагулянтами для предотвращения распространения тромбоза, восстановления венозной проходимости и снижения риска ТЭЛА или повторных тромбозов. Клинический опыт и ретроспективные когортные исследования доказали, что гепарин наиболее безопасный коагулянт при беременности, так как он не проникает через плаценту. Когортными исследованиями установлено, что риск выраженных кровотечений у беременных пациенток, леченных гепарином, составляет 2%. Гепаринотерапию следует начать у всех пациенток с дистальным тромбозом глубоких вен (например, вен голени), тромбозом проксимальных вен (например, подвздошно-бедренной или вен таза), и ТЭЛА. В одном из исследований небеременных пациенток сообщается о том, что 40% тромбозов вен голени остались изолированными, 40% лизировались и 20% распространились далее. Риск распространения у беременных, таким образом, должен быть существенным.
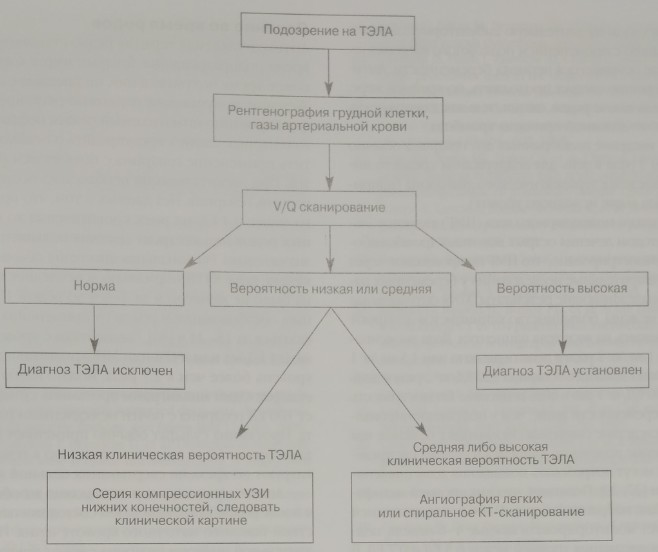
Рис. 12-2. Диагностика при подозрении на ТЭЛА во время беременности.
Так как терапевтические режимы для беременных пациенток разработаны недостаточно хорошо, гепаринотерапию следует начинать согласно существующим рекомендациям для небеременных пациентов [2, 26]. Тем не менее потребность в гепарине при беременности представляется повышенной, так как повышены концентрации гепарин-связывающих протеинов, объем плазмы и почечный клиренс. Гепарин при беременности относят к препаратам класса Б, он не экскретируется с грудным молоком. Первая задача антикоагулянтной терапии — обеспечение достаточно высоких доз с целью быстрого достижения терапевтических концентраций для минимизации опасности повторных тромбоэмболий. Лечение нефракциониро- ванным гепарином следует начать с внутривенного болюсного введения 5000 ЦЦ (80 ЕД/кг) с последующим переходом на постоянную инфузию по крайней мере 30 000 за 24 ч [2,27]. В качестве альтернативы гепарин можно начать дозировать по номограмме, основывающейся на весе пациентки, начиная с 18 ЕД/кг/час (табл. 12-2). Далее темп инфузии регулируют по лабораторным данным, таким как активированное частичное тромбопластиновое время (АЧТВ), международное нормализованное отношение (МНО) или уровень гепарина. Для гепарина как при ТГВ, так и ТЭЛА рекомендуются следующие целевые концентрации: АЧТВ, в 1,5-2,5 раза превышающее исходный показатель пациентки, МНО — в 2,5 раза, или концентрация гепарина 0,2-0,4 ЕД/мл.
Мониторинг гепаринотерапии осуществляют каждые 6 ч в первые 24-48 ч, а дозы подбирают по одной из стандартных номограмм для гепаринотерапии. Гепаринотерапию в виде постоянной инфузии можно продолжать 5-7 дней, с последующим переходом на длительную амбулаторную антикоагулянтную терапию с применением подкожного введения гепарина в течение оставшегося периода беременности. Антикоагуяянтиую терапию следует продолжать, по крайней мере, в течение 6 недель после родов, окончательная длительность лечения зависит от основной причины тромбоза.
Таблица 12-2. Дозирование антикоагулянтов3
- Гепарин 5000 ЕД внутривенно болюсно, далее 30 000 ЕД за 24 ч или
- Гепарин 80 ЕД/кг веса тела, далее 18 ЕД/кг/ч или
- Эноксипарин 1 мг/кг ПК 2 раза в день или 1,5 мг/кг в день или
- Дальтепарин 120 ЕД/кг ПК 2 раза в день или 200 ЕД/кг в день
3 Варфарин при беременности противопоказан.
Подкожное введение подобранных доз гепарина обычно назначают 2 пли 3 раза в день для поддержания среднего интервала АЧТВ в пределах терапевтического диапазона (например, в 1,5-2,5 раза выше исходного уровня).
Гагарины низкого молекулярного веса (НМГ) являются альтераптпвным методом лечения острых венозных тромбоэмболий. Ныло продемонстрировано, что НМГ не проникают через плаценту, — предварительные исследования у беременных пациенток дали обнадеживающие результаты. Хотя оптимальные дозировки пока не ясны, большинство клиницистов дозируют препарат, основываясь на весе тела пациентки. Доза эноксипа- рина составляет 1 мг/кг 2 раза в день подкожно или 1,5 мг/кг 1 раз в день подкожно. Доза дальтепарина 120 ЕД/кг 2 раза в день подкожно или 200 ЕД/кг 1 раз в день подкожно. Биодоступность НМГ в течение беременности выше, чем у нефракционированного гепарина, вследствие снижения связывания с белками; тем не менее повышение почечного клиренса и объема распределения препарата могут потребовать повышения дозы с течением беременности. Полагают, что пик уровней антифактора Ха (в пробах, набранных через 3-4 ч после последней инъекции) следует мониторировать каждые 4-6 недель, подбирая дозы для под держания уровней между 0,3 ЕД и 0,7 ЕД В последнее время высказываются предположения о том, что НМГ нс следует применять у беременных женщин с искусственными клапанами сердца вследствие недостаточной их эффективности у таких пациенток [30].
Варфарин не следует применять во время беременности вследствие его неблагоприятного влияния на развитие плода во время первого и второго триместров. Кроме того, варфа- рнн легко проникает через плаценту и может вызвать кровотечения у плода и новорожденного.
Венозная тромбоэмболия в послеродовом периоде
В послеродовом периоде лечение не отличается от такового у небеременных. Апарин внутривенно или НМГ начинают, как описано выше, а варфарин можно начать в первый день назначения гепарина. Терапию подбирают по уровню протромбино- вого времени, выраженного в виде МНО. У пациенток с венозной тромбоэмболией терапия должна быть подобрана так, чтобы поддерживать МНО в диапазоне от 2,0 до 3,0. Терапия варфарином производит быстрый антикоагулянтный эффект (вторичный быстрому снижению фактора V и протеина С) еще до достижения стойкого антитромботического эффекта (который отстает по крайней мере на 24-48 ч). Тем не менее важно продолжав гепаринотерапию или НМГ по меньшей мере еще 4 дня и не прекращать ее до тех пор, пока МНО не останется в пределах терапевтического диапазона в течение 2 дней подряд после начала лечения варфарином [26]. Лечение варфарином продолжают по меньшей мере в течение 3 месяцев с момента тромботического осложнения для минимизации риска рецидива. Лечение варфарином не противопоказано при грудном вскармливании. Так как применение варфарина во время беременности связано с риском дефектов плода, во время приема препарата должна быть обеспечена надежная контрацепция.
Лечение во время родов
Антикоагулянтная терапия редко становится проблемой во время родоразрешения. Гепарин имеет короткое, дозозависимое время полувыведения, нс зависящее от пути введения. Женщин, получающих подкожно регулируемые дозы либо фиксированно низкодозовый режим нефракционированного гепарина, следует предупредить о необходимости прекратить применение гепарина с появлением регулярных схваток. При госпитализации необходимо исследовать АЧТВ или уровень гепарина. Нет данных о том, что при уровне гепарина менее 0,4 ЕД/мл риск кровотечения во время влагалищных родов или кесарева сечения повышен сколько-нибудь значительно. Региональная анестезия обычно не противопоказана, если АЧ'ГВ нормально, а последнее введение гепарина было не менее чем за 4-6 ч до родов. Перед эпидуральным обезболиванием родов от применения НМГ следует отказаться за 18-24 ч [30]. Пациенткам с уровнем гепарина выше 0,4 ЕД/мл или АЧТВ или МНО повышающих контрольный уровень более чем в 2,7 раза, можно назначить протамина сульфат. Один миллиграмм протамина сульфата нейтрализует 100 ЕД гепарина с почти немедленным развитием эффекта. Протамина сульфат обычно применяют небольшими дозами (менее 50 мг вводят внутривенно в течение 10 минут) и титруют по времени свертывания цельной крови.
Антикоагулянтную терапию можно возобновить через 4-6 ч после родов, при стабильном состоянии пациентки и отсутствии тяжелого маточного кровотечения. При применении длительной инфузии гепарина следует повторно оценить выбранный режим после введения нагрузочной дозы 80 ЕД/кг. Лечение варфарином можно начать, как описано выше, в тот же день или как только пациентка будет в состоянии принимать лекарства перорально.
Тромболитической терапии у беременных пациенток следует избегать (за исключением жизнеугрожающих ситуаций) из-за опасности серьезного кровотечения у матери, особенно во время родов и сразу после них. Опасность преждевременной отслойки нормально расположенной плаценты и смерти плода вследствие применения этих препаратов выяснена не вполне. Фильтры нижней полой вены применялись у беременных женщин безопасно и эффективно. Их применение ограничено в основном группой пациенток с повторной ТЭЛА, развившейся несмотря на адекватную антикоагулянтную терапию, и тех, кому гепарин противопоказан из-за высокого риска осложнений, или имеющих в анамнезе патологическую реакцию на гепарин, как, например, гепарин-индуцированная тромбо- цитопения. Во избежание повреждений беременной матки рекомендуется установка на супраренальном уровне.
